Коллектив американских исследователей предложил использовать новый
полимерно-неорганический композит для лечения последствий инфаркта.
Несмотря на повышение качества медицинского обслуживания в развитых
странах, сердечно-сосудистые заболевания продолжают удерживать печальную
пальму первенства в списке причин смерти. Некоторые из заболеваний
требуют восстановления сердечных тканей, однако существующие
наноструктурированные материалы, например альгинат, используемые для в
качестве каркаса для восстановления таких тканей, обладают существенным
недостатком – весьма посредственной проводимостью, что не позволяет
восстановленному участку сердечной мышцы сокращаться / расслабляться
синхронно с неповрежденными тканями.
Рис. 1. Схематическое изображение структуры тканей, выращенных на
альгинатном каркасе (а) и на каркасе композита альгинат-золотые
нанонити.
Все дело в том, что пористая структура используемых каркасных
материалов препятствует прямому контакту между клетками, затрудняя
передачу электрических импульсов. Для обеспечения контакта между
разделенными клетками коллектив американских исследователей предложил
«навести мосты» золотых (выбранных из-за нетоксичности золота) нанонитей
(рис. 1), что отчетливо видно на СЭМ-микрофотографиях (рис. 2).
Увеличение проводимости было подтверждено измерением проводимости (для
чего пленка композита альгинат-нанонити была нанесено на подложку,
покрытую ITO) и импеданса (для чего все та же пленка была зажата между
двумя подложками, покрытыми ITO).
Рис. 2. Микрофотографии композитного материала, полученные с помощью ПЭМ и СЭМ.
Однако здесь можно задаться уместным вопросом – не будут ли
нанесенные нанонити препятствовать росту тканей на альгинатном каркасе?
Чтобы развеять все наши сомнения, авторы статьи извлекли клетки
кардиомиоцита и фибробласта из левого желудочка падшей смертью храбрых
лабораторной крысы и посеяли их на «чистый» альгинат и на композит.
Спустя три и восемь дней созревания (первые три в так называемых
стационарных условиях без внешнего электрического поля и последние пять с
ним) была обнаружена сильная флуоресценция тропонина I (белок,
участвующий в связывании ионов кальция и сокращении мышцы) в образце,
содержащем композит, но не в чистом альгинате (рис.3).
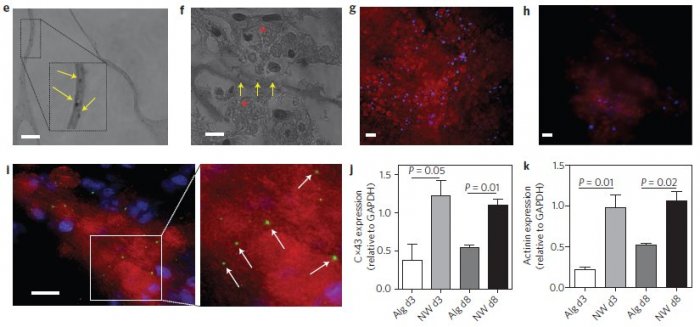
Рис. 3. Нанонити в «пустынной» (е) области каркаса и по соседству с
клетками (f). Сравните концентрацию тропонина в случае «чистого»(g)
альгината и композита (h), а также обратите внимание на распределение
коннексина 43 между кардиомиоцитами (i,j). Содержание коннексина 43 (j) и
саркомерного актинина (k) для обоих каркасов спустя 3 и 8 дней,
полученное с помощью вестерн блоттинга.
Вместе с тем, в «композитном» образце была обнаружена большая
концентрация коннексина-43 (белка образующего щелевые межклеточные
контакты, обеспечивающего синхронное сокращения сердечных клеток). Таким
образом,
добавление золотых нанонитей к альгинату не только способствовало
установлению полноценного электрического контакта между клетками, но
также обеспечило лучший механический контакт между каркасом и клетками.
Рис. 4. Сравните перераспределение концентрации ионов кальция в
различных точках (отмеченных римскими цифрами) при приложении внешнего
механического воздействия (в точке I). Обратите внимание, что в случае
чистого альгината концентрация ионов кальция меняется только в точке
приложения механического воздействия, в то время как в случае композита
концентрация меняется во всех контрольных точках синхронно. Белой
стрелкой изображено направление распределения волнового фронта
деполяризации клетки.
Поскольку в процессе сокращения/расслабления мышц существенно
изменяется концентрация ионов кальция, то по ее изменению можно судить о
синхронности сокращения / расслабления соседних клеток (рис.4).
Источник: Nature Nanotechnology

